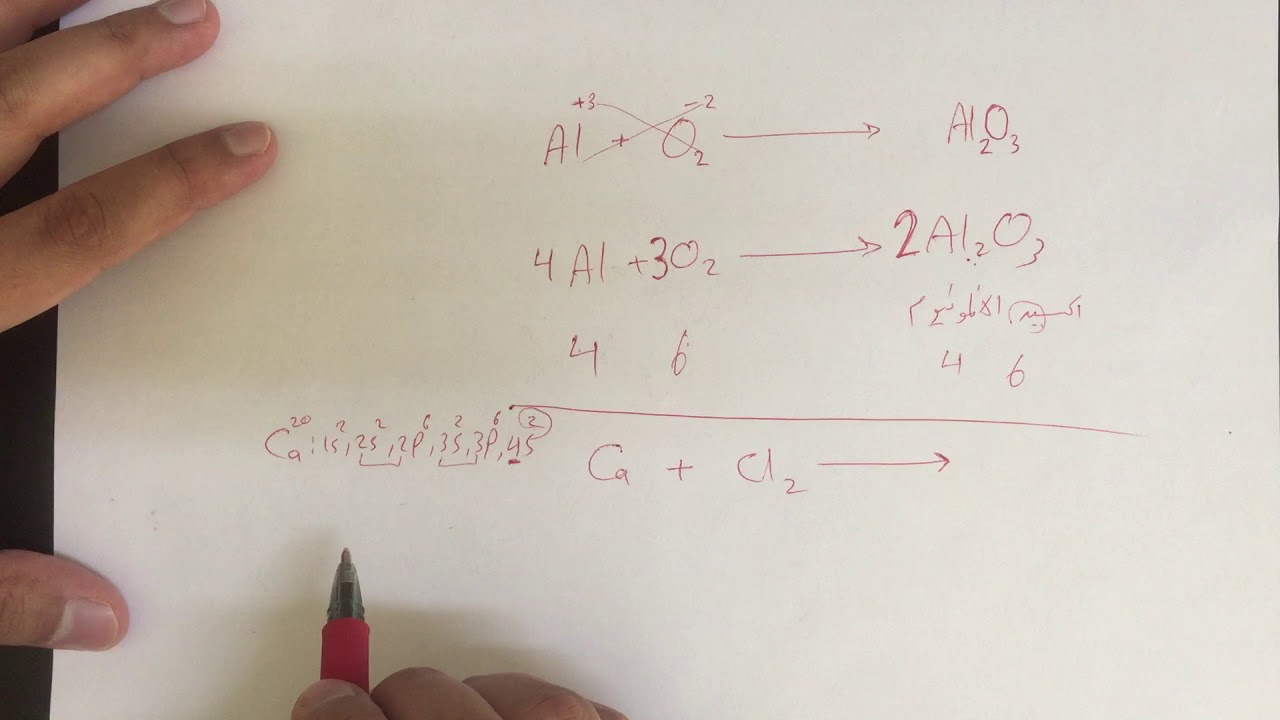صيغة المركب الأيوني الناتج من اتحاد الزوج التالي الكلوريد والكالسيوم هو - صيغة المركب الأيوني الناتج من اتحاد الزوج التالي : الألومنيوم والأكسيد هو

Recent Posts
- منتدى مسك الغلا
- هي باشة الغيد كلمات
- الطبيب المعجزه ٥٧
- صابون الغار الحلبي
- منصة مدد تسجيل دخول
- بيك رولز حراق
- افلام مايا خليفه تويتر
- الالف والواو تسمى علامات اعراب
- تبدأمهارةً تنطيط الكره من وضع الجلوس طولا
- غميم جدة حي مريخ
- Radhe torrent magnet
- امر اخلاء جزء ثاني الحلقه ١٣
- Pete davidson kim kardashian
- حل كتاب الانجليزي اول ثانوي مسارات 1.3
- كم عمر اليسا
- كود خصم وست الم
- بطة تسبح
- باب الجحيم
- اعراض لقاح كورونا
- دبل البيك
صيغ المركبات الأيونية
أردن 2000 الذرة التي لها أعلى كهروسالبية بين الذرات آلاتية هي أ 14Si ب 11Na ج 35Br د 17Cl 20.
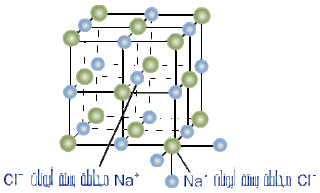
طبيعة بلوراتها صلبة وهشة تتمتع البلورات الأيونيّة بالصلابة وذلك بسبب قوى الجذب بين الأيونات الموجبة والسالبة إلى بعضهما وبالتالي يصعب فصلها، وعلى الرغم من ذلك إلّا أنّه عند الضغط على البلورة فإنَّ أيوناتها ذات الشحنات المتشابهة تقترب فيما بينها، ويعود سبب هشاشة المواد الأيونيّة الصلبة إلى وجود التنافر الإلكتروستاتيكي التنافر بين أزواج الإلكترونات الرابطة و غير الرابطة في الذرة والذي يُعدّ السبب الرئيسي لتقسيم البلورة.
على سبيل المثال ، يسمى F-1 الفلورايد ، لاسم العنصر الفلور.
اختاري
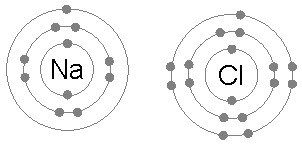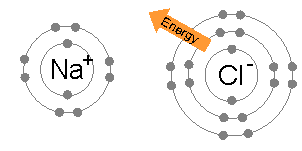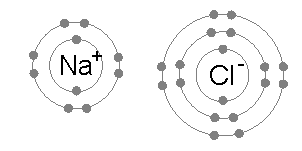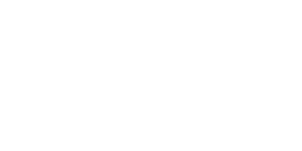
تتشكّل المركبات الأيونيّة نتيجة عملية فقد وكسب الإلكترونات بين الأيون الموجب الكاتيون مع الأيون السالب الأنيون للعناصر والتي ينشأ منها رابطة أيونية، وغالبًا يتمّ تكوين هذه المركبات عند تفاعل العنصر الفلزي القابل لفقد الإلكترونات ومع العنصر اللافلزيّ القابل لكسبها.
للمعالجة الكاملة ، انظر الرابطة الكيميائية: تكوين الروابط الأيونية.
تعتمد تسمية المركبات الأيونية على عِدّة قواعد منها؛ يجب كتابة الكاتيون أولاً يليه الأنيون في صيغة المركب، ويجب مراعاة نوع شحنة أيون الكاتيون إذا كانت موجبة أو متغيرة، ففي حال كانت موجبة يُكتب اسم نفس الأيون، بينما إذا كانت متغيرة يُكتب بدلالة الأرقام الرومانية، أمّا بالنسبة للأنيون إذا كان يمثل أيون أحادي الذرة فإنّه يُكتب بإضافة لاحقة 'يد' بجانب الاسم.
- Related articles
2022 www.conventioninnovations.com