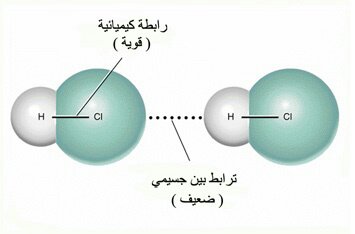
الروابط بين الجزيئات غير القطبية تسمى - شارح الدرس: الرابطة القطبية
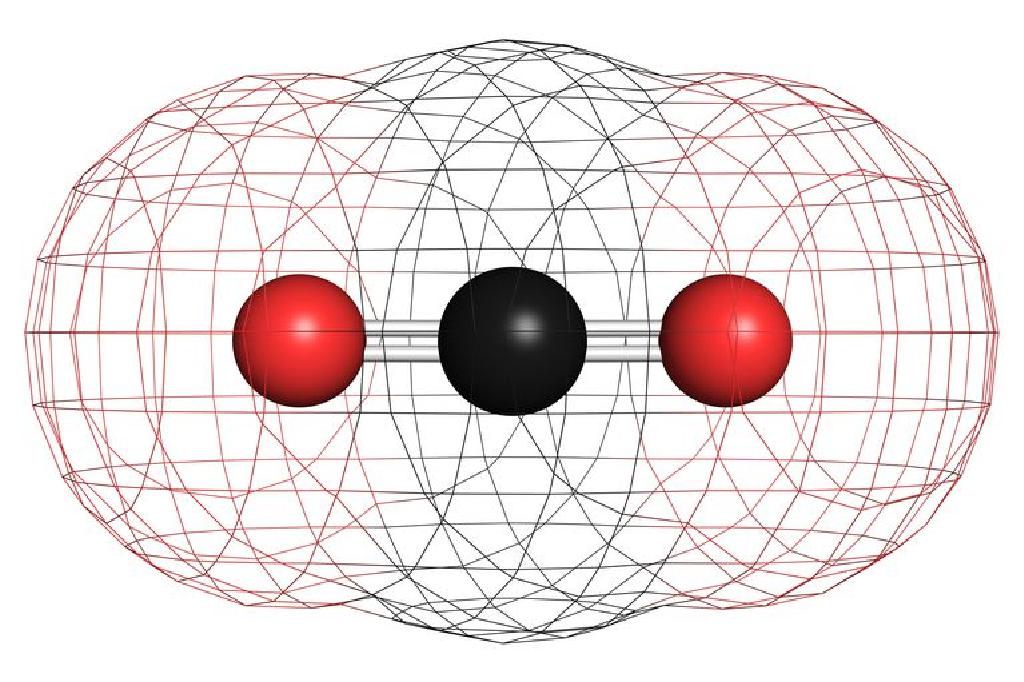
الكربون و الروابط بين جزيائته ايش
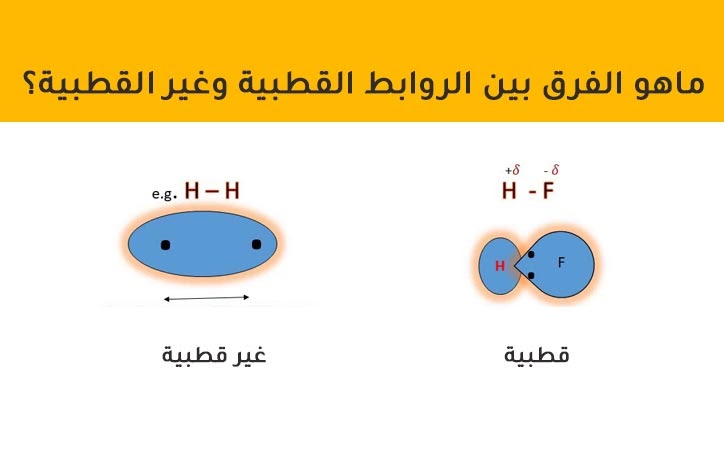
تجذب إحدى الذرات المرتبطة كمية غير متناسبة من الكثافة الإلكترونية، وتصبح الكثافة الإلكترونية مُركَّزة على أحد جانبَي الرابطة الكيميائية.
Taylor , 1975, Longman Group Limited , London.
نقل الإلكترون تسمى حركة الإلكترون باسم نقل الإلكترون، ولإنشاء الرابطة الأيونية يجب نقل الإلكترونات بين الذرات، فعلى سبيل المثال، يحتوي عنصر الصوديوم Na على إلكترون واحد فقط في غلافه الخارجي، لذلك فهو يميل إلى فقد هذا الإلكترون، بدلاً من استقبال 7 إلكترونات أخرى، وعندما يفقد هذا الإلكترون يترك شحنة موجبة قدرها +1 ، ويسمى بأيون الصوديوم، ومن ناحية أخرى، يحتوي الكلور Cl على 7 إلكترونات في غلافه الخارجي، لذلك فهو يميل إلى اكتساب إلكترون واحد، مما يجعله ذو شحنة سالبة -1 ، ويسمى بأيون الكلوريد.
- Related articles
2022 www.conventioninnovations.com





/schoolarabia/images/modules/chemistry/general_chemistry_im/level5/trabot_bean_algoze2at/atom14.gif)